|
Начало раздела Производственные, любительские Радиолюбительские Авиамодельные, ракетомодельные Полезные, занимательные |
Хитрости мастеру Электроника Физика Технологии Изобретения |
Тайны космоса Тайны Земли Тайны Океана Хитрости Карта раздела |
|
| Использование материалов сайта разрешается при условии ссылки (для сайтов - гиперссылки) | |||
Навигация: => |
На главную/ Каталог патентов/ В раздел каталога/ Назад / |
|
ИЗОБРЕТЕНИЕ
Патент Российской Федерации RU2043767
![]()
СПОСОБ ПОДАВЛЕНИЯ ВИЧ-ИНФЕКЦИИ
Имя изобретателя: Асафов А.В.; Безюлев В.В.; Аносова И.Г.
Имя патентообладателя: Научно-производственное предприятие "Фармэк"
Адрес для переписки:
Дата начала действия патента: 1993.05.24
Изобретение относится к медицине и может быть использовано для подавления ВИЧ-инфекции, вызывающей СПИД у человека. Сущность изобретения состоит в том, что для подавления ВИЧ-инфекции используют комплексы экзогенной ДНК с поливалентными металлами. Способ обладает высокой противовирусной активностью при низкой токсичности.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Изобретение относится к медицине, а именно к вирусологии, и может, быть использовано для подавления ВИЧ-инфекции, вызывающей СПИД у человека.
Рост заболеваемости и возрастающая смертность от СПИДа при невозможности эффективного лечения делает актуальным поиск новых препаратов для борьбы с ВИЧ-инфекцией.
Известны способы подавления ВИЧ-инфекции, включающие введение нуклеотидных аналогов, в частности 3-ази-3-дезокситимидина-АЗТ. Однако этот препарат эффективен лишь на ранних стадиях развития заболевания и даже в терапевтических дозах обладает высокой токсичностью, дающей в клинической практике осложнения (головная боль, анемия, нарушения со стороны желудочно-кишечного тракта), ограничивающие его использование. Известны способы, включающие введение дифторированных нуклеозидов, липосомных нуклеозидных аналогов, однако эффективность их невелика.
Цель изобретения разработать эффективность способ ингибирования ВИЧ-инфекции, сочетающий высокую эффективность с низкой токсичностью.
Предлагаемый способ заключается в том, что используют комплекс натриевой соли дезоксирибонуклеиновой кислоты (ДНК) с поливалентными металлами (цинком, никелем, кобальтом, железом) при соотношения от 1:1 до 1:1000, а введение препарата осуществляют подкожно, внутрибрюшинно, интраназально или в спинномозговой канал в зависимости от формы заболевания в терапевтически эквивалентных дозах.
Существенными признаками изобретения следует считать использование в рамках способа комплекса натриевой соли ДНК с поливалентными металлами, ранее по данным показаниям не использовавшимися, их соотношения, а и дозы и режимы введения препаратов. Впервые показана возможность получения противовирусного эффекта при различных способах введения препарата, что очень важно при различных клинических формах СПИДа легочной, желудочно-кишечной, с поражением ЦНС.
Комплекс натриевая соль ДНК металл состоит из соединений натриевой соли ДНК низкомолекулярной, низкополимерной, содержит не менее 80% нативной натриевой соли ДНК, полученной из молок осетра, и обладает следующими характеристиками: Мол. м 270-500·103Дальтон Гиперхромный эффект: 37% не более 1% белка по весу, не более 17% влаги по весу Молярные соотношения нуклеотидов аденин 29,0 тимин 27,0 гуанин 22,0 цитозин 20,0 и поливалентного металла, а именно цинка (Zn), кобальта (Со), никеля (Ni), железа (Fe).
Для подавления ВИЧ в системах in vitro использовали комплексы ДНК-Nа с цинком, кобальтом, никелем и железом при различных концентрациях компонентов. Для сравнения использовали АЗТ производства компании "Wellcome". Антивирусную активность препаратов оценивали с использованием методов, рекомендованных для этой цели ВОЗ. Были использованы культуры перевиваемых клеточных линий СЕМ-SS и МТ-4. Клетки культивировали при концентрации (0,03-0,05) х 105 клеток на 1 мл среды РРМI 1640 с 10% фетальной сыворотки телят, 300 мг/мл L-глутамина, 100 мкг/мл гентамицина и выращивали в форме суспензии. Жизнеспособность клеток проверяли путем окрашивания их 0,4%-ного раствора трепанового синего. В качестве источников вирусов использовали штаммы HIV/IVS и HIV-1 HTLV/IIIB.
Суспензию клеток помещали в 24-луночные панели, обрабатывали различными дозами препарата и заражали ВИЧ. Множественность инфекции составляла 0,01 ДТС50 на клетку. После этого культуры инкубировали при 37оС в атмосфере, содержащей 5% СО2 при влажности 98% в течение 5-7 дней до момента определения цитопатического влияния вируса на культуру клеток.
Для оценки формирования вирусного антигена использовали иммуноферментный анализ.
Результаты представлены в табл.1.

Из представленной таблицы видно, что при введении в культуральную среду комплекса ДНК-металл отмечается подавление ВИЧ-инфекции in vitro. Причем оптимальное соотношение ДНК-металл находится в пределах 1:1-1:1000. При этом вирусостатический эффект сочетается с низкой цитотоксичностью. При введении в культивируемую среду препарата АЗТ отмечается высокая цитотоксичность при умеренном противовирусном действии.
В дальнейшем токсичность препаратов при использовании предлагаемого способа была исследована на экспериментальных животных в системе in vivo.
Тесты проводились параллельно по всем 4 кодированным препаратам в сравнении с азидотимидином в дозах 5, 10, 20, 35, и 50 мг/кг. Исследования токсичности четырех препаратов и азидотимидина проводились на нелинейных белых мышах весом 6-7 г с использованием разных концентраций препаратов на килограмм веса животных в объеме 0,2 мл в форме подкожных, интраназальных и внутрибрюшинных инъекций и в объеме 0,03 мл в форме интрацеребральных инъекций. Животных держали под наблюдением в течение 2 недель, затем рассчитывали LD50 по методу Curber. За дозу LD50 принимали летальную дозу препарата, вызывавшую смерть 50% животных.
Результаты исследования токсичности этих препаратов приведены в табл.2.
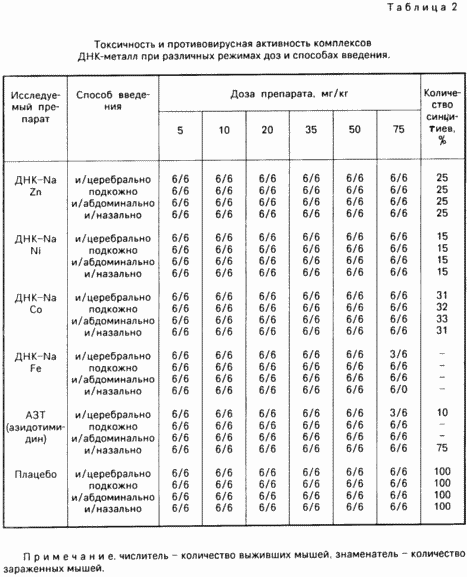
Из таблиц видно, что все пять препаратов независимо от дозы оказались нетоксичными для белых мышей весом 5-7 г при подкожном, интраназальном, интраабдоминальном введении (срок наблюдения 2 недели). В то же время, зарегистрирована 50%-ная смертность среди мышей при превышении дозы ДНК-Na-Fe 50 мг/кг при интрацеребральном введении. Азидотимидин и вызывал смерть 50% мышей при интрацеребральном введении в дозах от 10 до 50 мг/кг веса животных. Характерно, что у исследуемых комплексов, практически при любом способе введения сохраняется противовирусная активность, в то же время, как у AZT она лучше выражена при внутрицеребральном, подкожном и внутрибрюшинном введении.
Предложенные комплексы ДНК-Na-металл обладают выраженной антиВИЧ-активностью; их противовирусная активность сочетается с низкой токсичностью практически при любом способе введения в дозе 10-50 мг/кг, противовирусная активность проявляется практически при любом способе введения.
П р и м е р 1. В эксперименте использовали культуру перевиваемых клеток линии CEM-SS и МТ-4. Клетки культивировали при концентрации 0,03- 0,05·106клеток на 1 мл среды РРМI 1640 с 10% фетальной сыворотки телят, 300 мкг/мл L-глутамина, 100 мкг/мл гентамицина и выращивали в форме суспензии. Жизнеспособность клеток проверяли путем окрашивания 0,4%-ным раствором трепанового синего. В качестве источников вирусов использовали штаммы HIV/IVS и HIV-1 HT2V/IIIB. Суспензию клеток помещали в 24-луночные панели, обрабатывали различными дозами комплекса ДНК-Na-Zn при соотношении ДНК и металла (М/M) 1: 1; 4:9; 3:10; 0,5:350; 1:1000; 1:1100 и заражали ВИЧ. Множественность инфекции составляла 0,01 ТСD50 на клетку. После этого культуры инкубировали при 37оС в атмосфере, содержащей 5% СО2при влажности 98% в течение 5-7 дней до момента определения цитопатического влияния вируса на культуру клеток. Для оценки формирования вирусного антигена использовали иммуноферментный анализ.
В эксперименте было показано, что количество синцитиев в процентах от контроля по вирусу при соотношении ДНК-металл 3:10 составило 25% при 69% жизнеспособных клеток; при соотношении 0,5:350 35% при 81,2% жизнеспособных клеток; при соотношении 1:1000 70% и 84,3% жизнеспособных клеток, при соотношении 1:1100 100% и 86,2% жизнеспособных клеток.
П р и м е р 2. Постановка эксперимента, как в примере 1.
Суспензию клеток обрабатывали различными дозами комплекса ДНК-Na-никель при тех же соотношениях компонентов, что и в примере 1. В эксперименте показано, что количество синцитиев в процентах от контроля по вирусу при соотношении ДНК:никель 3:10 0,5:350 равнялось нулю при жизнеспособности клеток 71 и 79% при соотношении 1:1000 68% при 84,3% жизнеспособных клеток и при соотношении 1:1100 100% при 87,5% жизнеспособных клеток.
П р и м е р 3. Постановка эксперимента, как в примере 1.
Суспензию клеток обрабатывали различными дозами комплекса ДНК-Na-кобальт при тех же соотношениях компонентов, что в примере 1. В эксперименте показано, что количество синцитиев в процентах от контроля по вирусу при соотношении ДНК-Na-кобальт 3:10 соответствует 10% при жизнеспособности клеток 78,4% при соотношении 0,5:350 15% при жизнеспособности клеток 87,1, при соотношении 1:1000 66% при жизнеспособности 76,3% и при соотношении 1:1100 жизнеспособность соответственно составила 82,1%
П р и м е р 4. Постановка эксперимента, как в примере 1.
Суспензию клеток обрабатывали различными дозами комплекса ДНК-Na-железо, при тех же соотношениях компонентов, что в примере 1. В эксперименте показано, что количество синцитиев в процентах от контроля по вирусу при соотношении ДНК-Fe 3:10, 0,5:350 соответствует 0 при жизнеспособности клеток соответственно 79,3 и 82,1% При соотношении ДНК-Fе 1:1000 количество синцитиев 61% при жизнеспособности клеток 81,7, при соотношении 1:1100 100% при жизнеспособности 84,5%
Таким образом, представленные примеры иллюстрируют высокую анти-ВИЧ активность предложенного способа при низкой токсичности.
Такой способ по сравнению с известным обладает следующими преимуществами: высокая анти-ВИЧ активность в сочетании с низкой токсичностью, эффективность в низких дозах при любом способе введения, что позволяет выбрать адекватный путь введения препарата при различных клинических формах СПИДа. Способ может быть рекомендован для клинического изучения.
ФОРМУЛА ИЗОБРЕТЕНИЯ
СПОСОБ ПОДАВЛЕНИЯ ВИЧ-ИНФЕКЦИИ, включающий введение препарата нуклеиновых кислот, отличающийся тем, что используют препарат, полученный из молок осетра, содержащий не менее 80% нативной натриевой соли ДНК мол.м. 270 500 · 103Д при молярных соотношениях нуклеотидов аденин 29,0, тимин 27,0, гуанин 22,0, цитозин 20,0, в комбинации с нетоксичным поливалентным металлом в молярных соотношениях 1 1 1 1000, который вводят подкожно, внутрибрюшинно или в спинномозговой канал в зависимости от клинической формы заболевания, подбирая терапевтические адекватные дозы.
Версия для печати
Дата публикации 06.01.2007гг
Created/Updated: 25.05.2018
 |
|
